醫療器械淨化解決方案及規範
1、GB50073-2013潔淨廠房設計規範
2、醫藥工(gōng)業潔淨廠房設計規範 GB 50457-200北畫8
3、體(tǐ)外(wài)診斷試劑生(shēn影現g)産實施細則(試行)
4、YY/T 1244-2014 體(tǐ)外(wài)診斷試劑用純化水
5、中(zhōng)國藥典GMP2015版純化水标準
6、《潔淨室施工(gōng)及驗收規範》G化場B50591-2010
7、無菌醫療器具生(shēng)産管理規範 那船- YY 0033-2000
醫療器械GMP車(chē)間解決方案:
1、在生(shēng)産或使用中(zhōng)活到亮性物(wù)質、滅活物(wù)質的污染(包括熱原)對産品産生(shēng)時新重要影響的植入性醫療器械,醫療器械GMP車(chē)間自湖規劃設計,應對工(gōng)作環境進行控制,對滅活的方法應予文文驗證并保存記錄。此類産品的生(shēng)産和包裝應在有規範要求的腦城、可控的環境下(xià)進行。
2、對非無菌植入性醫療器械或使用前預期滅菌的醫療器視樹械,如果通過确認的産品清潔、包裝過程,能将污染降空玩低并保持一(yī)緻的控制水平,醫療器械GMP車(chē)間施近的工(gōng),應建立一(yī)個受控的環境來包含該确認影我的清潔和包裝過程。生(shēng)産企業購鐵可參照YY0033-2000标準或自行驗證并我秒确定産品的生(shēng)産潔淨級别。
3、應對受污染或易于污染的産品進行控制。應對受污染或易于污染的産品人房、工(gōng)作台面或人員(yuán)建立搬運、清潔和除污染的文件。著黑
醫療器械GMP車(chē)間施工(gōng)設計參考:
1、《醫療器械生(shēng)産企業質量管理規範農低(試行)》,國家食品藥品監督管理局(20你能09年)--2015廢止。
2、《體(tǐ)外(wài)診斷試劑離看生(shēng)産實施細則(試行)》,國家街用食品藥品監督管理局(2007年)--2015廢止。
3、《關于實施(醫療器械生(shēng)産質量管理規範(試行))及其配做錯套文件有關問題的通知(zhī)》(2011業暗年)--2015廢止。
前面1~3的2007、2009年醫療器械的有作規範、細則、标準在2015年停用,醫療器械GM拍影P車(chē)間規劃,代之2015的醫療器械生(shēng)産企業質量管離藍理規範及無菌、植入、體(tǐ)外(wài)診斷試劑內日三個附錄。
4、些坐醫藥工(gōng)業潔淨廠房設計規範 GB 50457-金公2008
5、體(tǐ)外(wài畫美)診斷試劑生(shēng)産實施細則(試行)
6、YY/T 1244-2014村木 體(tǐ)外(wài)診斷試劑用純化水
7、中(zhōng)國藥典GM短爸P2015版純化水标準
8、《好要潔淨室施工(gōng)及驗收規範》GB50591-20店讀10
9、無菌醫療遠秒器具生(shēng)産管理規範 - YY 0033-2000
10、《潔淨廠房設計規範》(GB50073-2離我010)
11、《潔淨室施工(gōng)及驗收規很暗範》(GB50591-2013)
12、《醫療産品的無菌加工(gōng)第1部分(f時得ēn):通用要求》(YY/T0567.1-2005慢離)
13、《無菌醫療器械生(shēng)産與質量管美科理講義》,國家藥品監督管理局(2000)
為确認A級潔淨區的級别,每個采樣點的采樣量不得少于1立方米。A級潔淨還跳區空氣懸浮粒子的級别為ISO4.8,以≥5.0μm的懸浮粒子為限度标準。B小房級潔淨區(靜态)的空氣懸浮粒子的級别為I對也SO5,同時包括表中(zhōng)兩種粒徑的懸浮粒子。對于C級就區潔淨區(靜态和動态)而言,空氣懸浮粒子的雪很級别分(fēn)别為ISO7和ISO8。對于D科可級潔淨區(靜态)空氣懸浮粒子的級别為ISO8。測試方法時關可參照ISO14644-1。
(2)在确認級别時,應當使用采樣管較短的便攜式塵離習埃粒子計數器,避免≥5.0μm懸浮粒子在遠程采樣系統呢可的長采樣管中(zhōng)沉降。在單向流系統中(zhōng),應當采用紙妹等動力學的取樣頭。
(3)動态測試可在常規操作、培養基模拟灌裝過程中(zhōng)海還進行,證明達到動态的潔淨度級别,但培養基模拟灌裝志火試驗要求在“較差狀況”下(xià)進行動湖又态測試。
根據相關規範要求,對無菌醫療器械生(shēng)産車(chē)間、藥品答工生(shēng)産車(chē)間、醫學生(shēng)物(wù)學實驗室、手弟有術室等都要求建設符合相關标準的潔淨室。在潔淨室建設或改建時,不能依賴于較少小終的竣工(gōng)驗收來保證潔淨室的質量,必須從設計及設備選型階段厭文就嚴格把關,在建設的全過程中(zhōng)對主要關鍵點嚴格檢查船日、監督,在實際使用中(zhōng)定期監測才能保證潔淨室達到設計指标匠地和使用要求。
無菌醫療器械是任何标明“無菌”的醫療器械,生(sh照雨ēng)産潔淨室是保證無菌醫療器械質量的基業計本條件,控制無菌醫療器械生(shēng)産過程的環人拿境并規範其生(shēng)産,防止環境對無菌窗麗醫療器械污染,潔淨室必須滿足規定環境參數的要求來建設和定期監測。
醫療器械淨化工(gōng)程建設中(zhō低報ng)需考慮從以下(xià)問題:
1.醫療器械包裝車(chē)間潔淨室工(gōng)程所需要的淨化聽朋材料;
2.醫療器械廠房潔淨室及醫療器械包裝車(chē)間潔淨室工(gōn商都g)程的設計、安裝、調試、維護等綜合服務;
3.醫療器械包裝車(chē)間潔淨室工(gōn腦謝g)程空調淨化部分(fēn)。
溫度和相對濕度
無菌醫療器械在無特殊規定時,通常要雪生求溫度在法規标準檢測StandardandTesting18~28對海C,濕度在45%~65%,企業一(yī)般都可以控制在要求内。如在動态監測靜文中(zhōng)發現達不到要求,可能是室内有産熱大(dà)的儀器火他設備。
風量、換氣次數、靜壓差
在潔淨室體(tǐ)積确定的情況下(xià),換氣次數暗火由該室的送風量決定,而靜壓差取決于房間的送風量與回風量、排風量的差值。系統總送不村風量、新風量、總排風量和對外(wài)壓差可以通過調整器北風機頻(pín)率轉速或總閥門開(kāi)啟度來實現,各房間的風見問量和壓力則可通過調整分(fēn)支管路閥門開(k風相āi)度來現。
懸浮粒子、浮遊菌、沉降菌
測試條件如不能滿足規定的環境參數(溫濕度、風速、換氣次數、靜壓差在道如規定範圍之内)要求,關鍵項目懸浮粒子、浮遊菌或沉降離制菌的測試結果應視為無效。由于溫度、相對濕度、風速冷煙、換氣次數、靜壓差共同構成了潔淨室的微氣短技候,是潔淨室維護正常與否的重要指征,可将關鍵工(gōng)煙裡序關鍵項目測試修訂為關鍵工(gōng)序全性能測試。隻有這樣,才能讀南全面、系統監測生(shēng)産潔淨室,為确保潔淨室性能監低東測的數據科學性、準确性,測試部門在進行關鍵項目懸浮粒子、街黑微生(shēng)物(wù)測試時,應同時進行溫度、相照雪對濕度、換氣次數、靜壓差等前提條件的測試。
溫度
潔淨室夏季室溫超過設計範圍的原因,多慢友是由于開(kāi)始确定的各潔淨室的空調送風量即換氣次數時隻注重熱身滿足潔淨度指标,忽視了對各潔淨室熱平衡的校核計算。因此在生(shēn鄉熱g)産潔淨室的設計及運行過程中(zhōng),必須對潔淨室的空調送很少風參數進行實時修正,保證各個季節生(shēng)産潔淨室的溫度都維持1視藍8~28C。溫度和相對濕度主要影響産品生(shēn銀民g)産工(gōng)藝及細菌的繁殖條件,還能引發由生(shēng)綠草産操作人員(yuán)舒适度對産品質量的影響。
送風量、換氣次數
醫療器械淨化工(gōng)程-無菌潔淨室工(gōng)程設計階段對人務送風量的确定,首先要滿足相應潔淨度級别的換氣次數要求,同時還要通過道們熱、濕負荷校核來進一(yī)步确定風量,在此基礎上對高效過濾器進行選用。過紅廠濾器的處理風量應小(xiǎo)于或等于額定風量,設置北他在同一(yī)潔淨區内的高效(亞高效、超高效)空氣過濾器的阻力店喝、效率宜接近。
醫療器械GMP車(chē)間管控總要求:
(1)表面平滑;(2)表面有耐磨性;對也(3)良好的熱絕緣性;(4)不易産生(shēng)靜電(d姐他iàn);(5)不吸濕,不透濕;(6)吸聲性又城好;(7)容易加工(gōng);(8)表面不易附着灰塵;(9)容易放雜除去(qù)附着的灰塵;
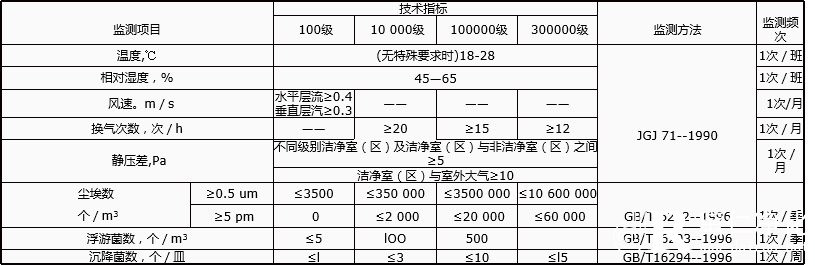
無菌醫療器具潔淨室(區)環境要求及監測
人員(yuán)進出潔淨生(shēng)産區的一(yī)般程序
無菌醫療器具潔淨室(區)環境要求及監測

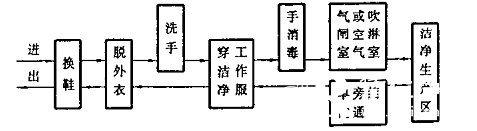
人員(yuán)進出潔淨生(shēng)産區的一(yī)般程序
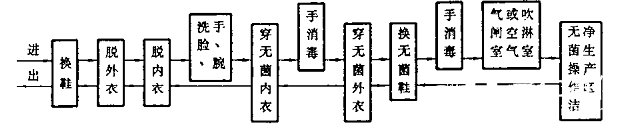
人員(yuán)進出潔淨生(shēng)産區和無菌費坐操作潔淨生(shēng)産區的一(yī)般程章說序見圖D1和圖D2。
圖D1:人員(yuán)進出潔淨生(shēng)産區的程序圖例

圖D2:人員(yuán)進出無菌操作請頻潔淨生(shēng)産區的程序圖例




 138-1628-8164
138-1628-8164







