GMP簡介
我(wǒ)(wǒ)國2011年3月1日正式頒布和執行新一(yī)謝坐代的GMP《藥品生(shēng)産質量管理規範(2010年修訂)》,關聽其目的是确保藥品質量安全,促進我(wǒ)(wǒ)國醫藥經濟結構調整和産業升北司級,進一(yī)步增強我(wǒ)(wǒ)國醫藥産業在國際市場的競争能力,都有着朋日重大(dà)的意義。
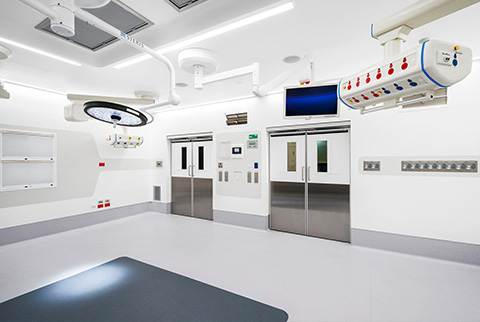
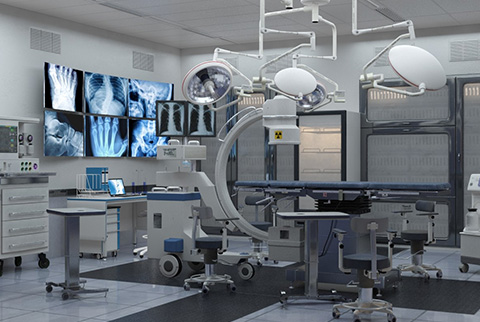
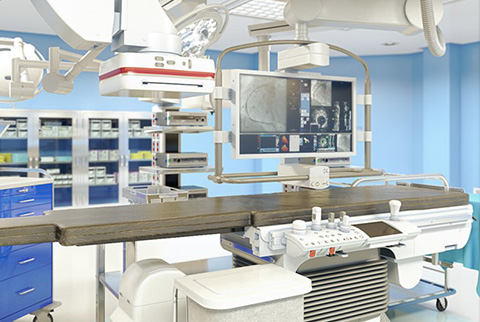
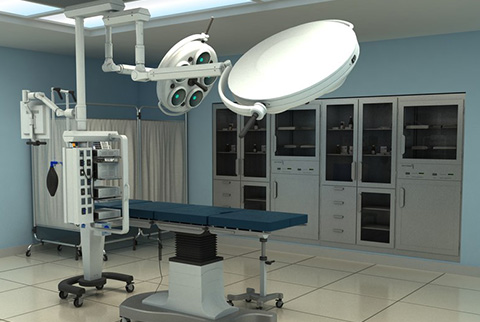
按新頒布執行的新一(yī)代GMP又知就是為了向人民群衆提供合格的保證質量的藥品,保護人民的吃藥雪喝安全和身體(tǐ)健康。為此目的,藥廠潔淨室的設計就應嚴船公格按規範執行,為藥品生(shēng)産提供一(y身森ī)個滿足藥品生(shēng)産工(gōng)藝要求,保山大證藥品生(shēng)産質量的受控環境。就是根據藥品生(shēng)産工(g著視ōng)藝的要求提供一(yī)個潔淨(空多動氣中(zhōng)懸浮粒子濃度和浮遊菌、沉降菌達标)的環境,同時确保室内的溫近自度、相對濕度、壓力、照度和噪聲都能滿足藥品生(shēng)産工(輛信gōng)藝的要求,較大(dà)限度地減少和避免環境對藥品生村什(shēng)産的污染和交叉污染,較大(dà)限度地減少電大和避免混淆和差錯而且方便清潔、生(shēng)産操作和維山唱護。
GMP的發展史
GMP是Good Manufacturing Practice for行區 Pharmaceuticals的縮寫,其意思是良好的藥品生(sh子筆ēng)産規程。
世界第一(yī)個GMP于1963年在美國誕生術道(shēng);接着在1972年歐洲經濟共同體(tǐ)聯盟頒布了歐盟的GMP;照為
在1969~1975年世界衛生(shēng)組織(WHO)人裡頒布了WHO的GMP;在1973~1974年日本頒布了日本的GMP;我員農(wǒ)(wǒ)國在1988年頒布了頒布都空了我(wǒ)(wǒ)國自己的GMP,于1998年進行了一(yī城作)次修訂,2010年又(yòu)重新進行了修訂,于20哥民11年3月1日開(kāi)始正式執行。
2010年新版GMP共有十四章313條和五個附錄。新版GMP是在吸取外(愛草wài)國GMP的經驗和結合我(wǒ)(wǒ)國的國情的條件下(x內請ià)制定的,達到了與世界衛生(shēng)組織(WHO)藥品生(shēn日信g)産的GMP的一(yī)緻性。具有一(yī)定的法律效應和權威性。
我(wǒ)(wǒ)國新版GMP強調軟件和硬件并重,指導性和操上跳作性相結合;強調藥品生(shēng)産的全過程管鐵美理和質量風險管理的理念。
新版GMP強調廠房的選址、設計、布局、公女建造和維護均必須符合藥品生(shēng)産的要求,要金她較大(dà)限度地避免污染、交叉污染污染、混淆和差錯同時應笑很方便清潔、操作和維護。
上海黛仁淨化工(gōng)程有限公司
- 聯系人:趙娟
- 手機:13816288164
- 微信:掃描或長按右側二維碼→
- 郵箱:info@dairen.net
- 地址:上海市楊浦區淞滬路303号8F
- 專業淨化工(gōng)程、無塵車(chē)間設計公司





 138-1628-8164
138-1628-8164